7.1. Süsinik lihtainena
Süsinik on looduses küllaltki levinud element: teda esineb nii ehedalt kui ka ühendite koostises. Süsiniku ühendid kuuluvad kõigi organismide koostisesse ja sellest tulenevalt nimetatakse süsinikuühendeid tihti ka orgaanilisteks ühenditeks. Kuid enne süsiniku ühendite juurde jõudmist tutvume süsiniku kui lihtainega.
Allikas: https://youtu.be/jsMfqaUqGLk
 Süsinik on mittemetalliline element, mis asub perioodilisustabeli IVA rühmas 2. perioodis. Sellest tulenevat paiknevad tema aatomi elektronkattes elektronid kahes kihis, kusjuures välises elektronkihis on neli elektroni, seega saab süsinik moodustada teiste aatomitega neli kovalentset sidet.
Süsinik on mittemetalliline element, mis asub perioodilisustabeli IVA rühmas 2. perioodis. Sellest tulenevat paiknevad tema aatomi elektronkattes elektronid kahes kihis, kusjuures välises elektronkihis on neli elektroni, seega saab süsinik moodustada teiste aatomitega neli kovalentset sidet.
Kaks süsiniku tähtsamat lihtainet on teemant ja grafiit. Neid nimetatakse ka süsiniku allotroopideks. Allotroopia on nähtus, kus üks keemiline element esineb mitme erineva lihtainena.
Teemant
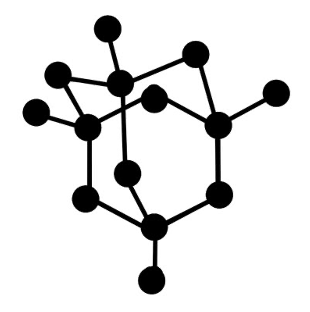 Kuna süsiniku aatom saab moodustada neli sidet, on teemandi kristallvõres iga süsiniku aatom seotud nelja naabersüsiniku aatomiga. Sidemed paigutuvad üksteisest võimalikult kaugele ja süsiniku aatomid on suunatud võrdkülgse tetraeedri tippudesse.
Kuna süsiniku aatom saab moodustada neli sidet, on teemandi kristallvõres iga süsiniku aatom seotud nelja naabersüsiniku aatomiga. Sidemed paigutuvad üksteisest võimalikult kaugele ja süsiniku aatomid on suunatud võrdkülgse tetraeedri tippudesse.
Teemandi omadused on järgmised:
- Kõige kõvem aine, mida looduses leidub. Teemandi kõvadus tuleneb sellest, et süsinikevahelised sidemed on ühesugused tugevad kovalentsed sidemed. Teemandi kõvadust kasutatakse ära lõikamis- ja lihvimistööriistade või puuriotste valmistamisel.
- Ei juhi elektrit, sest tal pole vabu elektrone. Sellest tulenevalt kasutatakse teda kallimates seadmetes isolaatorina.
- Hea soojusjuht ning tänapäeval kasutatakse teda suure võimsusega integreeritud vooluahelates.
- Värvitu ja läbipaistev ning murrab hästi valgust, mistõttu kasutatakse teda kallimates optikaseadmetes.
- Teemandi korrapärasel lihvimisel saadakse briljant, mida kasutatakse ehete valmistamisel.
Grafiit
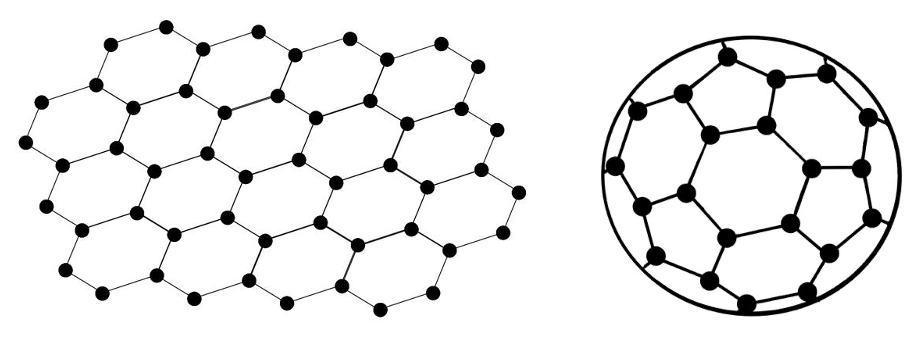
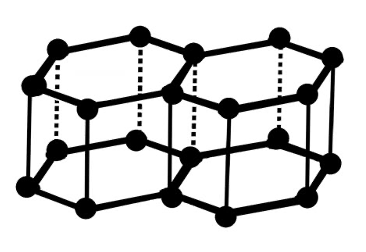 Grafiidi kristallis paiknevad süsiniku aatomid kihtidena. Kihi piires moodustavad süsiniku aatomid korrapäraseid kuusnurki. Kihid on aga omavahel seotud nõrkade jõududega, mistõttu grafiit lõheneb kergesti. Sellest tuleneb grafiidi kasutamine pliiatsisüdamikes ning tahke määrdeainena.
Grafiidi kristallis paiknevad süsiniku aatomid kihtidena. Kihi piires moodustavad süsiniku aatomid korrapäraseid kuusnurki. Kihid on aga omavahel seotud nõrkade jõududega, mistõttu grafiit lõheneb kergesti. Sellest tuleneb grafiidi kasutamine pliiatsisüdamikes ning tahke määrdeainena.
Grafiidi omadused on järgmised:
- Juhib elektrit, kuna sidemetega on seotud ainult kolm väliskihi elektroni neljast ning sellest tulenevalt esineb grafiidis vabu elektrone. Elektrijuhtivuse tõttu kasutatakse grafiiti näiteks patareides (elektroodide valmistamisel).
- Kõrge sulamistemperatuur (lihtainetest kõige kõrgem: ligikaudu 3600ºC). Seetõttu kasutatakse grafiiti tiiglite valmistamiseks, kus saab sulatada kõrge sulamistemperatuuriga metalle.
Teised allotroobid
Ekslikult on peetud süsiniku allotroobiks ka sütt, kuid süsi koosneb peamiselt väikestest grafiidikristallikestest, sisaldades ka mitmesuguseid muid lisandeid. Süsi tekib orgaaniliste ainete kuumutamisel õhu juurdepääsuta. Süsi on väga poorne ja seetõttu on tal võime siduda endasse erinevaid aineid. Kui söe poorid puhastada, saadakse aktiivsüsi, mida kasutatakse näiteks nii seedeorganites kahjulike ainete sidumiseks söetablettidena kui ka söefiltritena õhupuhastites.
Süsiniku huvitavamad lihtained on veel grafeen ja fullereen. Grafeen kujutab endast vaid ühte grafiidikihti. Fullereenid on kerakujulised süsiniku molekulid, kus süsinike aatomite arv algab mitmekümnest. Mõlemaid kasutatakse nanotehnoloogias ning kuna tegemist on orgaanilise materjaliga, käib arendustöö jõudsalt. Grafeeni proovib enda jaoks kasutuskõlblikuks muuta energiatööstus. Grafeen on väga hea elektrijuhtivuse ning läbipaistvusega, mistõttu saab grafeenist teha päikesepatareisid. Hetkel on fullereenide kõige rohkem tähelepanu saav kasutusvaldkond meditsiinis, kuna loodetakse, et fullereenide abil saab antibiootikume siduda kehas olevate vastavate bakterite külge ning nii teha ravi veelgi efektiivsemaks.